Що не так із російською вакциною проти коронавірусу. Головне
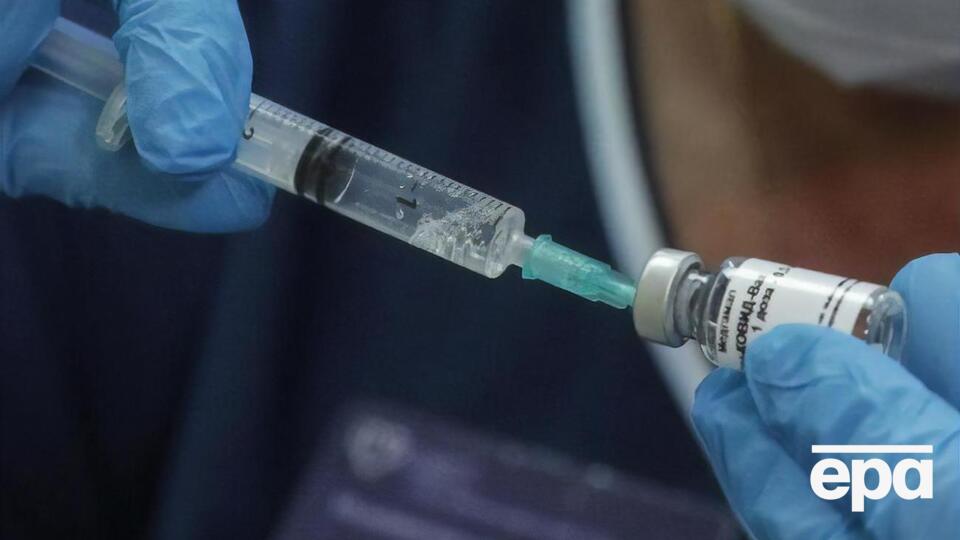
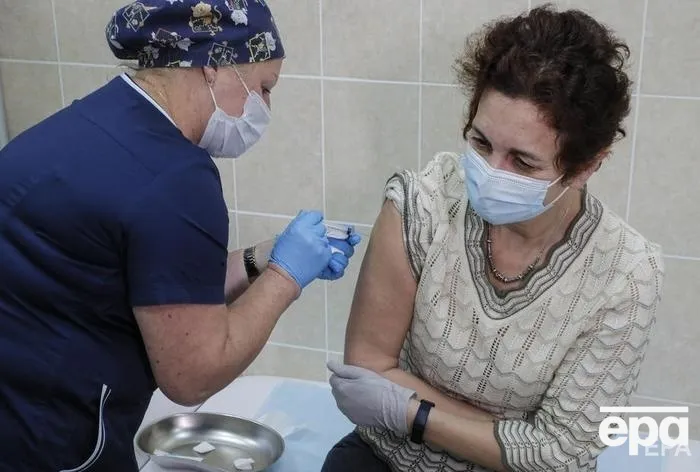
Масове щеплення російською вакциною планують розпочати 2021 року
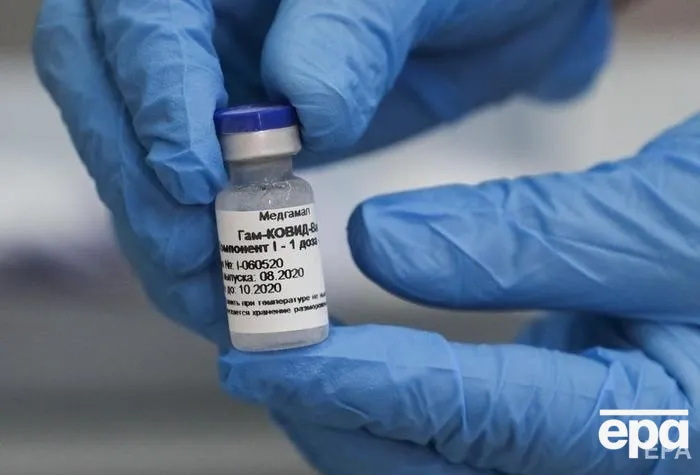
Фото: EPA
У серпні президент РФ Володимир Путін заявив про реєстрацію першої у світі вакцини проти коронавірусу "Супутник V". Він говорив, що вакцина "працює досить ефективно", і розповів, що щеплення зробила його донька. Водночас сам Путін не вакцинувався. За словами спікера Кремля Дмитра Пєскова, президент "не може брати участь у випробуваннях". Вакцина зазнала критики з боку наукової спільноти передусім через те, що пройшла лише дві фази клінічних випробувань, а третю розпочали вже після її реєстрації. Група добровольців заявляла про побічні реакції після щеплень. Розробники препарату стверджують, що в тих, хто щепився, сформувалися антитіла. "ГОРДОН" розповідає, що відомо про вакцину "Супутник V" і чому її критикують.
Що це за вакцина?
У серпні президент РФ Володимир Путін оголосив про реєстрацію "першої у світі вакцини проти коронавірусу" з назвою "Супутник V".
"Учора вранці вперше у світі зареєстровано вакцину проти нової коронавірусної інфекції... Я знаю, що вона працює досить ефективно, формує стійкий імунітет і витримала всі необхідні перевірки", – заявив Путін.
Він сказав, що вакцинували його доньку.
За словами міністра охорони здоров'я РФ Михайла Мурашка, Національний дослідницький центр епідеміології та мікробіології імені Гамалії МОЗ Росії розпочав розроблення вакцини "одразу ж після того, як Всесвітня організація охорони здоров'я оголосила пандемію". Він стверджував, що за результатами доклінічних і клінічних досліджень вакцина "засвідчила високу ефективність і безпечність".
"В усіх добровольців сформовано високі титри антитіл COVID-19. Водночас у жодного з них не зафіксовано серйозних ускладнень імунізації", – заявляв Мурашко.
На сайті вакцини вказано, що її "можна використовувати для щеплення населення в Росії".
Розробники стверджують, що другий, проміжний, аналіз даних клінічних випробувань засвідчив ефективність вакцини на рівні 91,4% на 28-й день після першої дози, а за 42 дні після першої дози ефективність перевищує 95%.
Зараз вакцина доступна для повнолітніх громадян РФ, які знають російську мову (щоб заповнити всі документи), пише РБК. Масову вакцинацію для решти розпочнуть 2021 року, вона буде добровільною.
24 листопада спікер Кремля Дмитро Пєсков заявив, що Путін не щеплювався цією вакциною, оскільки не може бути добровольцем у випробуваннях.
"У нас же не розпочали ще широкої вакцинації, і як доброволець, звісно, глава держави не може брати участі у вакцинації. Просто як глава держави він не може добровольцем брати участь – це неможливо", – цитує Пєскова РБК.
Чому критикують "Супутник V"
Критика російської вакцини пов'язана переважно з тим, що її зареєстрували до проходження третьої фази клінічних випробувань. Як пише National Geographic, випробування третьої фази мають вирішальне значення для перевірки готовності вакцини до поширення. Цей фінальний крок у тестуванні призначено для встановлення найбезпечнішої дози для широкого використання (це можна з'ясувати тільки введенням вакцини різнорідній групі з тисяч людей). Ця стадія розроблення вакцини також визначає ступінь її ефективності.
11 серпня МОЗ РФ видало тимчасову реєстрацію на препарат до 1 січня 2021 року, пише РБК.Якщо під час тестування на великій вибірці вакцина продемонструє негативні наслідки, реєстрацію можуть відкликати.
Коментуючи реєстрацію вакцини на цьому етапі, директор НДІ імені Гамалії Олександр Гінзбург сказав BBC: "Пандемія – це і є надзвичайна умова, коли гинуть люди, як на війні. Тому наш уряд ухвалив цю постанову, і вона дає єдину можливість: низку необхідних процедур для реєстрації проводити не послідовно, а паралельно, що заощаджує дуже велику кількість часу".
У першій і другій фазах випробувань, які провели на вакцині на момент реєстрації, брало участь по 38 добровольців. Голова відділення лабораторної медицини Каролінського медичного інституту у Стокгольмі Матті Сельберг заявив агентству "РИА Новости", що, якщо вакцину випробували на 76 людях, складно говорити про показники її ефективності або побічні ефекти.
4 вересня в науковому журналі The Lancet розробники вакцини опублікували статтю з результатами першої та другої фаз випробувань. У ній автори заявили, що препарат "переносять легко", він "викликає сильну гуморальну і клітинну імунну відповідь у 100% здорових учасників".
Згодом група із 40 учених, серед яких були й російські, опублікувала відкритий лист на адресу журналу The Lancet. Вони вимагали більше інформації про дослідження. Науковцям здалося дивним, що графіки рівня антитіл у випробовуваних різних груп у різні дні дуже схожі. Розробники вакцини відповіли публікацією в The Lancet. Вони стверджують, що дані наведено в початковому вигляді, а всі збіги пов'язані з тим, що дослідження проводили серед невеликої кількості учасників. Нових даних вони не опублікували.
У коментарі "Русской службе BBC" один з авторів листа, професор біології американського Університету Темпл Енріко Буччі заявив, що вченим не дали навіть доступу до оригінальних даних дослідження.
"Тобто вони залишають за собою право відмовляти в доступі до даних – це абсолютно неприйнятно!" – сказав він.
Ще один автор листа, докторант Північно-Західного університету у США Костянтин Андрєєв, заявив BBC, що теж помітив низку невідповідностей у статті російських учених.
"Ми маємо намір звернутися до редакції The Lancet і домогтися запиту на публікацію цього клінічного протоколу, щоб незалежна група вчених могла проаналізувати повні дані й хоча б переконатися в тому, що їх не сфальсифіковано", – сказав він.
У коментарі "Немецкой волне" Андрєєв розповів, чому вирішив зробити запит розробникам російської вакцини на більший обсяг даних.
"Перше, що мені здалося дивним, коли я прочитав статтю в The Lancet, – що вибірка пацієнтів для цього дослідження становить лише 76 осіб, по 38 – на кожну фазу. Для порівняння, під час другої фази клінічних випробувань вакцини, яку розробляє компанія AstraZeneca спільно з Оксфордським університетом, було залучено понад тисячу учасників. Також бентежить відсутність контрольної групи, якій вводили плацебо, і те, що дослідження не охоплювало вікових груп пацієнтів, найбільш схильних до побічних явищ", – сказав учений.
Також, за його словами, незрозуміло, чи було дотримано часового інтервалу між першою і другою фазами дослідження, і чому результати дослідження оприлюднили, не чекаючи закінчення 180-денного строку спостережень, як заявили самі розробники у протоколах клінічних випробувань.
"Так, найбільшу кількість запитань викликає розподіл незалежних один від одного експериментальних значень одразу на кількох графіках. Наприклад, рівень різних типів Т-лімфоцитів (CD4 і CD8) у дев'яти пацієнтів із дев'яти виявився абсолютно ідентичним. Аналогічна картина – і з повторюваним розкидом концентрацій антитіл у різних пацієнтів. Водночас даних цитометрії, на підставі яких будували графіки і які могли б висвітлити це питання, наразі у відкритому доступі немає. Для порівняння: до раніше згаданої статті про вакцину Оксфордського університету і AstraZenecа додано додаткові матеріали з вихідними даними на понад 100 сторінках", – сказав він.
Андрєєв зазначив, що "цілковито унеможливити збіги не можна".
"Однак імовірність цього приблизно така сама, як у всіх дев'яти осіб, зібраних в одній кімнаті, виявити однакове співвідношення довжини пальців ніг із кількістю волосся на голові. Ця величина становить приблизно соті частки відсотка", – сказав учений.
Як пише "Русская служба BBC", 10 вересня в Російському фонді прямих інвестицій заявили, що опубліковані дані "є достовірними та точними і пройшли експертизу у п'ятьох рецензентів The Lancet, а повнорозмірний клінічний протокол надавали до редакції журналу".
Прессекретар фонду Арсеній Палагін заявив, що подано "повний звіт про проведення дослідження, 300 сторінок". Однак "Русская служба BBC" звернула увагу, що публікацію російських науковців у The Lancet супроводжує лише 22-сторінковий документ із приміткою про те, що саме в такому вигляді його було прикладено до надісланої в редакцію оригінальної статті і передано експертам для рецензії.
"Куди зникла решта нібито переданого до редакції 300-сторінкового звіту, невідомо", – ідеться в матеріалі.
"Відсутність прозорості результатів доклінічних або клінічних випробувань, не кажучи вже про прозорість самої процедури, як і раніше, викликає занепокоєння", – заявив Томас Куней із Міжнародної федерації фармацевтичних виробників та асоціацій.
Український педіатр Євген Комаровський заявив, що поки що невідомо, наскільки гарною чи поганою може бути російська вакцина проти коронавірусу.
"На це запитання відповіді немає. Причому ще раз кажу: не гарна і не погана. Вона недоношена поки що, але зараз у процесі активного доношування. Її активно тестують, купі людей її вводять. Ми, можливо, за пів року, вісім місяців приблизно знатимемо, який у цих усіх тисяч людей, яким її ввели, рівень імунітету, які є реакції побічні. Я як лікар юридично не маю права її рекомендувати, тому що вона не пройшла в повному обсязі клінічних випробувань", – сказав він в інтерв'ю засновнику інтернет-видання "ГОРДОН" Дмитрові Гордону.
Чеська молекулярна вірусологиня Рут Тахезі в інтерв'ю "Радіо Свобода" розповіла, що не робила б щеплення вакциною "Супутник V", як і будь-якою іншою, яка не пройшла всіх фаз випробувань.
"Про "Супутник V" у журналі The Lancet було опубліковано статті про результати першої та другої фаз клінічних випробувань. Але результати здобули після випробувань на вкрай низькій кількості учасників – і це викликає підозри, тому що професіонали зазвичай не практикують такого в разі випробування вакцин... Я не думаю, що в неї [вакцини] зовсім немає шансів на успіх пройти і завершити всі етапи клінічних випробувань, третю фазу. Але мене дивує невідповідність міжнародній практиці, що "Супутник V" у Росії вже застосовують, незважаючи на відсутність результатів третьої фази випробувань. Я б вакциною, яка не пройшла третьої фази клінічних випробувань, ніколи не робила щеплення... Якщо зараз цією вакциною прищеплюють більшу кількість людей, я бажаю, щоб після неї в людей не виникли ускладнення. Це може бути вкрай небезпечно", – заявила Тахезі.
Вона зазначила, що деякі побічні ефекти можна виявити тільки після випробувань на великій кількості людей. Окрім того, розробники російської вакцини не досліджували її дії в різних вікових групах.
"Це [реєстрація вакцини до закінчення третьої фази випробувань] небезпечний прецедент. Якби щеплення так стали застосовувати повсюдно, це могло б бути дуже небезпечним. Прискорений режим у таких випадках неможливий [...] Доки вакцину не випробують на великій кількості людей, не можна встановити, спричиняє вона хвороби чи погіршує перебіг уже наявних. Останнє є важливим у разі людей старшого віку, які зазвичай мають якісь хронічні захворювання. Ігнорувати ці правила можна лише в разі, якщо ми зіткнемося з еболою чи пташиним грипом, які мають майже 60-відсоткову смертність. Тільки в цьому випадку кожному з нас є сенс зробити щеплення вакциною, що становить ризики, – щоб не померти", – підкреслила Тахезі.
Головний інфекціоніст США, директор Національного інституту алергії та інфекційних захворювань Ентоні Фаучі заявляв у серпні National Geographic, що серйозно сумнівається в тому, що російська вакцина готова до широкого застосування. Він підкреслив, що створення вакцини не дорівнює доказу її ефективності та безпеки.
"Я сподіваюся, що росіяни дійсно остаточно довели, що вакцина безпечна й ефективна. Я маю серйозні сумніви, що вони це зробили", – сказав він.
Фаучі зазначив, що інші компанії також розробляють вакцини і вони вже пройшли перші фази випробувань, але їх не дозволяють широко застосовувати без проходження третьої фази.
"У нас є пів дюжини чи більше вакцин. Тож, якби ми хотіли ризикнути, нашкодити великій кількості людей або дати їм щось, що не працює, ми могли б почати робити це й наступного тижня, якби захотіли. Але це не так", – сказав він.
Побічні ефекти і випадки захворювання
Третю фазу клінічних випробувань російської вакцини "Супутник V" розпочали 9 вересня. За планами, у випробуваннях має взяти участь 40 тис. осіб, із них 10 тис. введуть плацебо.
Директор НДІ імені Гамалії Гінцбург заявляв, що у 85% тих, хто зробив щеплення, не фіксували побічних ефектів, пише РБК. За його словами, серед імовірних побічних реакцій – підвищення температури до 38 градусів, іноді головний біль, ломота у м'язах і почервоніння на місці уколу.
"Це стандартні прояви для всіх вакцин", – сказав він.
Деякі добровольці, які випробували вакцину на третьому етапі, заявили про різні побічні реакції. Зокрема, медіаменеджер Андрій Василенко розповів, що після першого щеплення в нього підвищилася температура, а згодом почалися проблеми із серцем.
"І збити температуру було майже неможливо. Парацетамол летів просто в нікуди. 40,2 – і все тут. Пульс – 140–160. Лихоманка сильна, електричні грілки від стану, коли морозить, який супроводжував лихоманку, узагалі не допомагають – зігрітися вкрай складно", – заявив він.
Василенко у Facebook заявляв, що телефонував у НДІ імені Гамалії, але йому відповіли: "Чого ви сюди телефонуєте? Ми не маємо жодного стосунку до досліджень вакцини. Не відволікайте нас від роботи. Якщо у вас є запитання, то зайдіть на сайт і там їх ставте через спеціальну форму!"
"У підсумку звернувся у приватну клініку. Дійсно виявили проблеми із серцем, яких до сьогодні взагалі не було (зокрема й за дослідженнями піврічної давнини). І є деякі побоювання щодо виникнення міокардиту (запалення серцевого м'яза). Плюс я вперше побачив у своєму аналізі крові значення С-реактивного білка (показника запалення) 61.26 мг/л (за норми від 0 до 5 мг/л). Такого в мене не було ніколи", – заявив він.
Департамент охорони здоров'я Москви в коментарі "Уралінформу" назвав симптоми Василенка "неприємними, але абсолютно безпечними й такими, що минають самі".
"Я зараз можу сказати однозначно: я своїм батькам у жодному разі не радитиму цієї вакцини. Зараз можу її рекомендувати тільки в тому разі, якщо у вас є знайомі лікарі чи якась клініка, де ви лікуєтеся, і ви твердо впевнені, що, якщо у вас виникнуть якісь ускладнення, вас відразу туди заберуть і почнуть лікувати", –розповів він "Радіо Свобода".
Про побічні ефекти й відчуття після щеплення РБК розповіли інші добровольці.
"Протягом перших двох днів після щеплень фіксували підвищення температури до 38,5 ºС і ломоту в тілі. Упродовж наступних днів симптоми зникли повністю. Досвід оцінюю як позитивний. Незважаючи на вищеописані проблеми, імунітет сформовано, і я задоволений", – сказав адвокат Олег Єлісєєв.
Ведуча жіночих тренінгів Катерина Дорогова повідомила, що після першої ін'єкції в неї була температура 37,5 ºС. "З'явилося щось схоже на піломоторний рефлекс, це те, що дехто називає "аж тіло терпне". Лягла спати раніше, уночі відчувала середнє потовиділення, а вранці все чудово, наче нічого не було", – зазначила вона.
Доцент Московської консерваторії Філіп Нодель заявив, що не відчув жодних симптомів після введення препарату. Він висловив надію, що йому ввели не плацебо. Добровольці стверджувати, що за результатами аналізів у них сформувалися антитіла, але на різному рівні.
Окрім побічних ефектів, були також випадки захворювання на COVID-19 серед добровольців. Троє медиків в Алтайському краї захворіли на COVID-19 після того, як їм зробили щеплення проти коронавірусу, писав сайт amic.ru. Головна епідеміологиня Алтайського краю Ірина Переладова заявила, що "щодо жодного щеплення немає гарантій того, що людина після нього не захворіє, тому що вона може перебувати в інкубаційному періоді". За її словами, перед вакцинацією лікарі робили тести на коронавірус і на антитіла, й вони були негативними. Вона припустила, що лікарі могли заразитися між взяттям матеріалу для тестування і вакцинацією.
Розробники вакцини поспішили запевнити, що лікарі заразилися коронавірусом до того, як почав діяти імунний захист, котрий з'являється протягом кількох тижнів після щеплення, пише "Радіо Свобода".
Гінцбург також заявляв, що в деяких добровольців були позитивні результати тесту на коронавірус. Він припустив, що ті, хто заразився, могли бути одними з тих, кому вводили плацебо.
Що говорить ВООЗ
Після оголошення про реєстрацію російської вакцини Європейське бюро Всесвітньої організації охорони здоров'я заявило, що почало перемовини із РФ.
"Ми непокоїмося через безпечність та ефективність не тільки російської вакцини, але й усіх вакцин, які наразі у стадії розроблення", – заявила старша представниця Європейського регіонального бюро ВООЗ із надзвичайних ситуацій Кетрін Смоллвуд, повідомляє Voice of America.
За словами голови бюро Ганса Клюге, незважаючи на те, що винахід вакцини – це гарна новина, усі мають пройти однаково ретельну перевірку.
Голова ВООЗ Тедрос Адханом Гебреєсус у вересні заявив, що організація не рекомендуватиме будь-яких вакцин, доки не переконається в їхній безпечності, писало агентство Associated Press.
"Я хотів би запевнити громадськість, що ВООЗ не підтримуватиме вакцини, яка не є ефективною і безпечною", – сказав він.
Ситуація з мером Ялти
18 жовтня помер "мер" окупованої Ялти Іван Імгрунт. Як писав "Коммерсантъ", причиною стало ускладнення тромбозу на тлі COVID-19.
Про госпіталізацію Імгрунта із пневмонією стало відомо 30 вересня. Тоді він оцінював свій стан як нормальний.
Інформація про те, що Імгрунта вакцинували російською вакциною "Супутник V", з'явилася в різних джерелах після його смерті. Зокрема, як повідомляє проєкт "Радіо Свобода" "Крим.Реалії", про це у Facebook писав ялтинський блогер і журналіст Євген Гайворонський, якого окупанти раніше звинувачували у вживанні психотропних засобів і "депортували" на материкову Україну. Зараз публікація за цим посиланням у соцмережі недоступна. "Крим.Реалії" пише, що, за словами блогера, Імгрунт "для піару робив щеплення проти коронавірусу російською вакциною".
У "Крим.Реалії" зазначили, що Імгрунт нічого не говорив про вакцинацію, а його "колеги" з окупаційної адміністрації "підтвердити цю версію не змогли".
Сайт "Цензор.НЕТ" із посиланням на неназвану публікацію у Facebook, яка зараз недоступна, також писав, що Імгрунт "для піару" зробив собі щеплення проти COVID-19" в один час із нардепом від "Опозиційної платформи – За життя" Віктором Медведчуком під час приїзду того в Ялту.
"Російські лікарі хворобу Імгрунта пов'язують саме з ускладненням від вакцини", – цитував сайт публікацію соцмережі.
Низка українських ЗМІ писала про вакцинацію Імгрунта з посиланням на матеріал агентства "Укрінформ", яке посилалося на новину видання "Моя семья". Зокрема, це сайти "Остров" і "Новости Краматорска".
На сайті "Укрінформу" лінк, який вказали у своїх матеріалах "Остров" і "Новости Краматорска", зараз веде на порожню сторінку. На сторінці "Укрінформу" в Telegram зберігся пост із лінком на недоступну зараз новину із заголовком "Мер Ялти помер від COVID-19 після російської вакцини, яку рекламував Медведчук – ЗМІ".
Сайт GreenPost писав про вакцинацію Імгрунта з посиланням на неназвані російські ЗМІ.
Окупаційне "МОЗ" Криму спростовувало інформацію про вакцинацію Імгрунта.
"У зв'язку з поширенням користувачами соціальних мереж і Telegram-каналами недостовірної інформації міністерство охорони здоров'я Республіки Крим офіційно повідомляє, що голову адміністрації міста Ялта Івана Івановича Імгрунта, який перебував на лікуванні й помер в одному з лікувальних закладів Санкт-Петербурга, не вакцинували проти нової коронавірусної інфекції COVID-19", – заявили у "відомстві".
На якому етапі розроблення інших вакцин у світі
На сьогодні, за даними ВООЗ (.pdf), у світі проходить випробування 48 вакцин – кандидатів проти коронавірусу, жодної з них поки що не схвалено.
Третю фазу випробувань завершили компанії Moderna і Pfizer. Вакцина mRNA-1273 компанії Moderna продемонструвала ефективність на рівні 94,5% за підсумками третьої фази.Moderna має намір протягом найближчих тижнів подати заявку в Управління із санітарного нагляду за якістю харчових продуктів і медикаментів США (FDA) для надання дозволу на застосування вакцини в екстрених ситуаціях. FDA оцінить вакцину на підставі спостереження за 151 учасником випробувань, яке триватиме два місяці.
Компанія Pfizer 18 листопада оголосила про 95% ефективності вакцини BNT162b2 проти COVID-19, створеної спільно з німецькою BioNTech.
Як читати ”ГОРДОН” на тимчасово окупованих територіях
Читати