Тодуров: Люди просто не бачили, які тромбози бувають у пацієнтів із COVID-19. А ризику утворення тромбів від вакцини ніде не доведено

Тодуров: Вакцина, яку сьогодні завезено в Україну, ліцензована
Фото: Borys Todurov / Facebook
Противники вакцинації дуже сильно ризикують своїм життям і життям людей, яких вони агітують не вакцинуватися, підкреслив гендиректор Інституту серця Борис Тодуров.
Чутки, що вакцина проти коронавірусу може спричинити ризик тромбозу, не доведені, а тромби можуть утворюватися і в пацієнтів, які хворіють на COVID-19. Про це в ефірі ток-шоу "Свобода слова Савіка Шустера" на каналі "Україна" 19 березня заявив гендиректор Інституту серця Борис Тодуров.
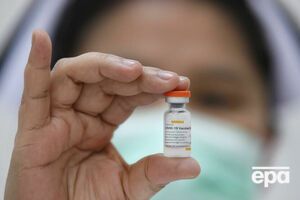
"Вакцина, яку сьогодні завезено в Україну, ліцензована (йдеться про вакцину від Oxford/AstraZeneca (Covishield), виготовлену в Індії за ліцензійною угодою. – "ГОРДОН"). Компанія, яка її виробляє, робить вакцини на 60% усього світового ринку, це дуже серйозна, потужна компанія. Наскільки мені відомо, вакцину, яку привезли в Україну, купили дуже розвинені країни, такі як Канада, наприклад, і багато інших. Говорити про її ефективність або неефективність на сьогодні ми поки не можемо, тому що немає статистики. Але те, що від неї не так багато ускладнень, я вже зараз можу сказати, тому що співробітники нашого інституту провакцинувалися, 64 людини позавчора одержали перші дози вакцини. І практично ні в кого не було жодних реакцій, крім невеликої субфебрильної температури у двох осіб", – заявив Тодуров.
Лікар зазначив, що противники вакцинації дуже сильно ризикують своїм життям і життям людей, яких вони агітують не вакцинуватися.
На прохання прокоментувати чутки про ризик тромбозу після вакцини Тодуров заявив: "Люди просто не бачили, які тромбози бувають у тих, хто хворіє на COVID-19".
"Якщо комусь цікаво, я запрошую до нас у реанімацію. Ми заведемо й покажемо, які важкі пацієнти у нас на 100-відсотковому кисні, на вентиляції, молоді, у 38 років, умирають. Умирають від задухи, захворівши на COVID-19. Ось це тромбози. А те, що викликає вакцина, – це не тромбози, це легка температура. Ніде не доведено сьогодні, що ця вакцина викликає підвищене тромбоутворення. Тож поки це все на рівні фантазій і контраргументів для так званих антивакцинаторів", – додав він.
Україна використовує виготовлену в Індії за ліцензійною угодою вакцину розроблення AstraZeneca під назвою Covishield.
Більше ніж 10 країн останніми днями заявили про зупинення застосування вакцини проти коронавірусу AstraZeneca або окремих її партій. Зокрема, в Данії з'явилися повідомлення про випадки тромбозу у пацієнтів, яким ввели вакцину. Інші держави заявляли, що таких випадків не фіксували, проте зупиняють вакцинацію цим препаратом як запобіжний захід.
Комітет з оцінювання ризиків фармаконагляду Європейського агентства з лікарських засобів 18 березня заявив, що переваги вакцини AstraZeneca в боротьбі з коронавірусною інфекцією все ще переважають ризики. Такі висновки було зроблено після завершення попереднього розгляду повідомлень про тромби в людей, щеплених вакциною AstraZeneca.
Схожу заяву 18 березня зробили у британському Агентстві з регулювання лікарських засобів і медичних виробів, а 19 березня – у Всесвітній організації охорони здоров'я. Після цього країни почали відновлювати вакцинацію препаратом від AstraZeneca.
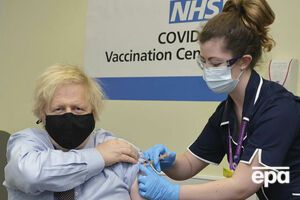
4 січня Великобританія першою у світі почала масову вакцинацію препаратом від AstraZeneca. Постійний комітет із вакцинації Stiko при Інституті вірусології імені Роберта Коха в Німеччині 28 січня рекомендував використовувати вакцину від AstraZeneca громадянам віком від 18 до 64 років.
EMA 29 січня дозволило застосування вакцини проти COVID-19 виробництва AstraZeneca на території Європейського союзу. Цього самого дня постачання вакцини на території ЄС схвалила Єврокомісія.
В агентстві зазначили, що клінічні дослідження вакцини проти коронавірусу AstraZeneca засвідчили, що вона ефективна в запобіганні COVID-19 у людей віком від 18 років. Ефективність вакцини встановлено на рівні приблизно 60%.
Як читати ”ГОРДОН” на тимчасово окупованих територіях
Читати