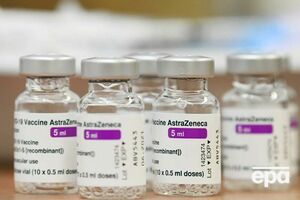
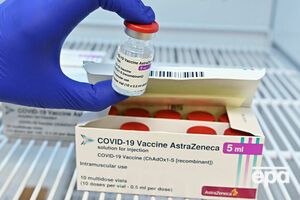
Дослідження у США, Перу й Чилі продемонстрували 100-відсоткову ефективність вакцини AstraZeneca проти тяжких форм COVID-19 і підтвердили її безпечність – компанія

У людей віком від 65 років ефективність вакцини становила 80%, зазначили в компанії AstraZeneca
Фото: EPA
Незалежна комісія з моніторингу безпечності даних не виявила підвищеного ризику тромбозу в понад 21 тис. учасників дослідження, яким ввели хоча б одну дозу AZD1222, повідомили в компанії AstraZeneca.
Вакцина проти коронавірусу AZD1222 розроблення компанії AstraZeneca і Оксфордського університету повністю запобігає тяжким формам захворювання на COVID-19. Про це свідчать результати третьої фази клінічних випробувань препарату у США, Перу та Чилі, повідомляють на сайті AstraZeneca 22 березня.
Дослідження, у якому взяло участь 32 449 осіб, продемонструвало 100-відсоткову ефективність вакцини у випадках тяжкого перебігу COVID-19. Водночас ефективність препарату проти коронавірусу становить 79%. Зазначають, що в людей віком від 65 років ефективність вакцини була вищою – 80%.
У процесі дослідженні його учасникам вводили дві дози препарату з інтервалом у чотири тижні. Збільшення інтервалу введення другої дози вакцини може ще більше підвищити її ефективність, зазначили в AstraZeneca.
Водночас незалежна комісія з моніторингу безпечності даних (DSMB) не виявила підвищеного ризику тромбозу або випадків, пов'язаних із тромбозом, серед 21 583 учасників, яким ввели хоча б одну дозу AZD1222, ідеться в повідомленні.
"Ці дані підтверджують попередні результати, зафіксовані під час випробувань AZD1222 серед дорослого населення, але приємно вперше побачити такі результати ефективності серед людей віком понад 65 років", – підкреслила професорка Медичної школи Університету Рочестера (США) Енн Фолс.
Понад 10 країн заявляло про зупинення застосування вакцини проти коронавірусу AstraZeneca або окремих її партій. Зокрема, у Данії з'явилися повідомлення про випадки тромбозу в пацієнтів, яким ввели вакцину. Інші держави заявляли, що таких випадків не фіксували, проте зупиняють вакцинацію цим препаратом як запобіжний захід.
Комітет з оцінювання ризиків фармаконагляду Європейського агентства з лікарських засобів (ЕМА) 18 березня зазначав, що переваги вакцини AstraZeneca в боротьбі з коронавірусною інфекцією все ще переважають над ризиками. Такі висновки зробили після завершення попереднього розгляду повідомлень про тромби в людей, щеплених вакциною AstraZeneca.
Таку заяву 18 березня зробили у британському Агентстві з регулювання лікарських засобів і медичних виробів, а 19 березня – у Всесвітній організації охорони здоров'я.
Після цього країни почали поновлювати вакцинацію препаратом AstraZeneca.
4 січня Великобританія першою у світі почала масову вакцинацію препаратом AstraZeneca. Постійний комітет із вакцинації Stiko при Інституті вірусології імені Роберта Коха в Німеччині 28 січня рекомендував використовувати вакцину AstraZeneca громадянам віком від 18 до 64 років.
EMA 29 січня дозволив застосування вакцини проти COVID-19 виробництва AstraZeneca на території Європейського союзу. Цього самого дня постачання вакцини на території ЄС схвалила Єврокомісія. В агентстві зазначали, що клінічні дослідження вакцини проти коронавірусу AstraZeneca продемонстрували, що вона ефективна в запобіганні COVID-19 у людей віком від 18 років. Ефективність вакцини було встановлено на рівні приблизно 60%.
Як читати ”ГОРДОН” на тимчасово окупованих територіях
Читати