BioNTech и Pfizer запросили разрешение на применение их вакцины в Евросоюзе для детей в возрасте 5–11 лет

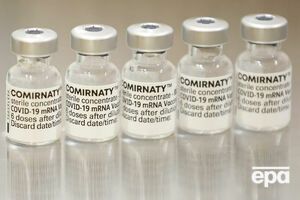
В исследовании вакцины Comirnaty приняли участие 2268 детей в возрасте от шести месяцев до 11 лет, отметили в BioNTech
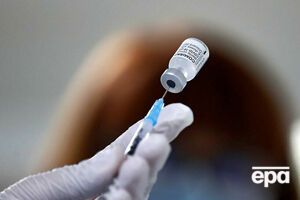
Фото: EPA
Pfizer и BioNTech предоставили Европейскому агентству по лекарственным средствам (EMA) результаты исследования об иммунизации детей в возрасте от пяти до 11 лет препаратом от COVID-19 Comirnaty, компании хотят получить разрешение на продажу их вакцины в ЕС. Об этом говорится в пресс-релизе компании BioNTech, опубликованном 15 октября.
Те же данные были отправлены в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA).
Отмечается, что в исследовании вакцины приняли участие 2268 детей в возрасте от пяти до 11 лет.
Для них использовали меньшую дозу, чем обычно вводят взрослым.
Pfizer и BioNTech заявили, что результаты исследований показали "сильный иммунный ответ".
20 сентября компания Pfizer сообщала, что вакцина Comirnaty эффективна для детей в возрасте от пяти до 11 лет. Эффективность препарата проверяли в трех возрастных группах: 5–11 лет, два – пять лет, шесть месяцев – два года.
Контекст
- Вспышка коронавирусной инфекции началась в конце 2019 года в Китае. 11 марта 2020 года Всемирная организация здравоохранения объявила распространение коронавируса пандемией.
- 10 мая FDA расширило перечень людей, которым можно в экстренном порядке прививаться вакциной против коронавируса производства Pfizer/BioNTech, включив в него подростков 12–15 лет. 13 мая в США началась вакцинация детей в возрасте 12–15 лет.
- США стали второй страной, одобрившей препарат Pfizer/BioNTech для детей, первой аналогичное решение приняла Канада. Препарат одобрили после того, как 31 марта Pfizer и BioNTech заявили о 100% эффективности своей вакцины от COVID-19 для подростков 12–15 лет.
Как читать ”ГОРДОН” на временно оккупированных территориях
Читать