Европейский регулятор одобрил вакцину Moderna от коронавируса
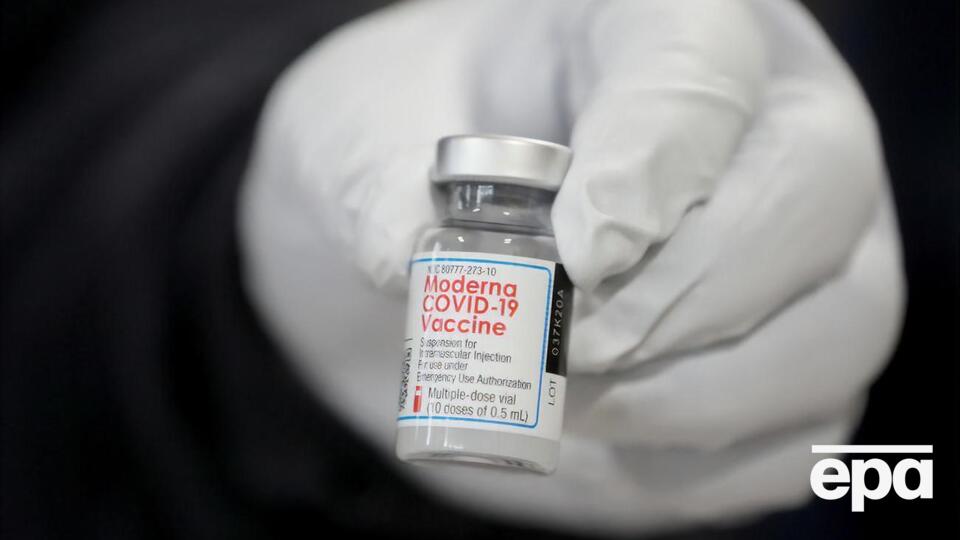
Вакцина от Moderna показала 94,1% эффективности против коронавируса
Фото: EPA
Европейское агентство по лекарственным препаратам рекомендовало Европейской комиссии выдать американской компании Moderna разрешение на продажу ее вакцины от коронавируса в Евросоюзе.
Европейское агентство по лекарственным препаратам (EMA) одобрило вакцину против коронавируса американской компании Moderna для использования на территории Евросоюза, говорится на сайте агентства.
"Комитет EMA по лекарственным средствам для человека тщательно изучил данные о качестве, безопасности и эффективности вакцины и на основе консенсуса рекомендовал Европейской комиссии выдать формальное условное разрешение на продажу", – говорится в сообщении.
В агентстве отметили, что клинические исследования вакцины от Moderna показали, что она эффективна в предотвращении COVID-19 у людей от 18 лет. Эффективность вакцины установлена на уровне 94,1%.
Исследования также показали эффективность препарата на уровне 90,9% у пациентов с риском тяжелого течения COVID-19, в том числе с хроническими заболеваниями легких, сердечными заболеваниями, ожирением, заболеваниями печени, диабетом или ВИЧ-инфекцией.
Вакцина от Moderna вводится в виде двух инъекций в руку с интервалом 28 дней. Наиболее частые побочные эффекты вакцины были легкими или умеренными и исчезли в течение нескольких дней после вакцинации. Среди них: боль и припухлость в месте инъекции, усталость, озноб, лихорадка, увеличение или болезненность лимфатических узлов в подмышках, головная боль, боль в мышцах и суставах, тошнота и рвота.
Это вторая вакцина, которую EMA рекомендовало разрешить для использования в ЕС. Первой в декабре стала вакцина от немецкой компании BioNTech и американской Pfizer. 27 декабря в Евросоюзе официально стартовала массовая вакцинация этим препаратом.
Вспышка коронавирусной инфекции началась в конце 2019 года в Китае. 11 марта 2020 года Всемирная организация здравоохранения объявила распространение коронавируса пандемией.
Как читать ”ГОРДОН” на временно оккупированных территориях
Читать